Reaktion Calciumcarbonat mit Wasser (& Natriumhydrogencarbonat mit H20)?
Erläutern sie die Beobachtungen der beiden Versuche durch Anwendung der Säure Base Theorie nach Brönsted (auch unter Angaben von Reaktionsgleichungen)
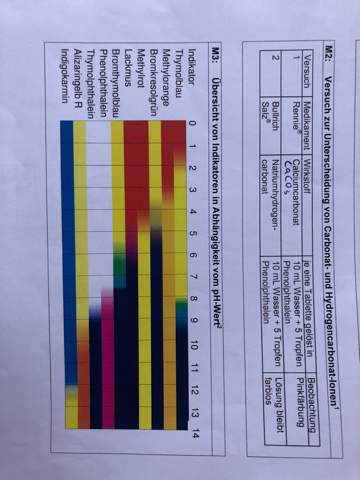
2 Antworten

Ich gehe jetzt nicht auf Säure oder Base ein:
Das Kalziumkarbonat ist ein Salz, das sehr wenig löslich ist. Eigentlich ist es so gut wie gar nicht in Wasser löslich. Das erklärt man mit dem Löslichkeitsprodukt.
Das Natriumhydrogenkarbonat = Natron = Speisesoda:
Es löst sich gut im Wasser, die Lösung ist annähernd pH-neutral. Das kann man ohne Schaden trinken. Manche hochwertigen Mineralwasser haben einen hohen Anteil an Natriumhydrogenkarbonat gelöst = Staatl. Fachingen.
---------------------------------------------------------------------------------------------------------------------
Anmerkung OT: Das Kalziumhydrogenkarbonat ist merklich in Wasser löslich. Das ist ein Teil der Temporären Härte im Leitungswasser und im Grundwasser. Es ist oft im Mineralwasser enthalten (Longlife - Radkersburger). Man kann auch sagen, die Kohlensäure hat etwas Kalk gelöst.

Na, erst mal kommt ganz allgemein die Definition einer Säure/Base nach Bronsted, dann die beiden Dissoziationsgleichungen und eine Überlegung zu starken und schwachen Säuren und Basen und ihren korrespondierenden schwachen und starken Basen und Säuren.
Und schon ist die Erklärung für das pinke oder farblose Phenolphtalein da. ;-)
m.f.G.
anwesende

Calciumcarbonat löst sich als Hydrogencarbonat und Calciumhydroxid, aber nur sehr wenig. Daher ist die Lösung nicht alkalisch, obwohl sie es von der Theorie sein müsste (Salz aus starker Lauge und schwacher Säure)
Das Natriumhydrogencarbonat löst sich zu Kohlensäure (also CO2 und H2O) und Natronlauge, ist aber deutlich weniger alkalisch als Natriumcarbonat. Trotzdem ist die Lösung alkalisch genug für das Phenolphtalein.
Ich hatte die Reaktionsgleichung richtig aufgestellt, aber bei beiden war das eine Produkt falsch. Hast du eine Idee, welche Produkte rauskommen? :)