PH Wert und Konzentration?
Okay, ich bin maximal verwirrt.
Wenn man einen PH-Wert von zum Beispiel 13 hat, ist es alkalisch. Hat es dann 0,0000000000001 mol pro Liter von dem Stoff H3O+ ?
H3O+ kennzeichnet doch saure Lösungen.
was ist wenn etwas PH1 ist und die Konzentration von OH- bei 0,1 mol/L liegt? Ist es dann eine saure Lösung??
1 Antwort

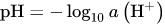
Der pH Wert ist die logarithmische Konzentration der H+ Ionen.
DER REST GILT NUR FÜR WÄSSRIGE LÖSUNGEN!
Auch stark basische Lösungen enthalten etwas H3O+ - aber deutlich mehr OH-. Andersrum gilt das genauso. Auch starke Säuren enthalten OH-, aber DEUTLICH mehr H3O+
Wasser hat einen pH-Wert von 7. Hier liegen also 1*10^-7 mol/L an H3O+ Ionen vor. Berechnet man den pOH Wert von Wasser (genau das selbe wie der pH Wert, nur für OH- Ionen), kommt das gleiche raus.
- Wenn stead einen PH-Wert von zum Beispiel 13 hat, ist es alkalisch. Hat es dann 0,0000000000001 mol pro Liter von dem Stoff H3O+ ?
Ja.
- H3O+ kennzeichnet doch saure Lösungen
Nur wenn es mehr H3O+ als OH- gibt. Ist der pH Wert >7, ist die Lösung basisch, bei pH < 7 ist es sauer und pH = 7 ist neutral. H3O+ ist überall, die Konzentration ist aber immer anders.
- was ist wenn etwas PH1 ist und die Konzentration von OH- bei 0,1 mol/L liegt? Ist es dann eine saure Lösung??
das geht nicht. Wenn der pH-Wert bei 1 ist, die Konzentration von OH- bei 1*10^-3 mol/L- Die Konzentration von H3O+ ist bei 1*10^-1 mol/L --> 0,1 mol/L.
Die Lösung ist bei einem pH wert von 1 sauer.
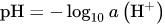

Okay danke, wieso sagt man bei Neutralisationsreaktionen zum Beispiel dass eine alkalische Lösung mit der c= 0,1 mol/l vorliegt?

Ich habe eine neue Frage gestellt, da kannst du sehen was ich meine :)