Wo erkenne ich ob die Ionen positiv oder negativ sind?
Ich habe hier eine Tabelle, jetzt meine frage: wie erkenne ich ob es positiv oder negativ ist?
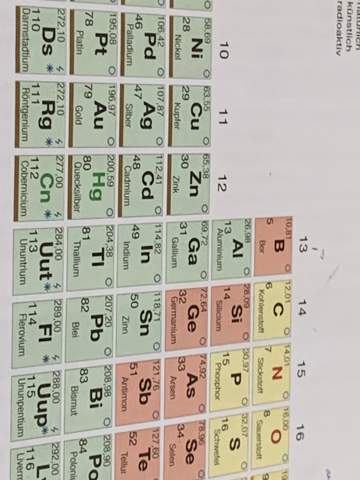
Danke & liebe grüße❤️
2 Antworten

Du zeigst hier das Periodensystem der chemischen Elemente. Die Atome hier sind alle neutral. Positiv und negativ geladene Atome gibt es erst, wenn sie eine Verbindung miteinander eingehen. Beispiel
Natrium hat ein Elektron auf seiner äußersten Schale
und will ein Elektron abgeben.
Chlor hat sieben Elektronen auf seiner äußersten Schale
und will ein Elektron aufnehmen .
Wenn die beiden ihr Geschäft besiegelt haben, ist Chlor um ein Elektron (also eine negative Ladung) reicher, also negativ geladen und Natrium ist ein Elektron losgeworden und ist jetzt positiv geladen.
Ungleichnamige Ladungen ziehen sich an und son haben wir jetzt eine Verbindung aus Natrium und Chlor, also Natriumchlorid, Kochsalz.

Hi,
das ist keine Tabelle, sondern das PSE. Alle Atomsorten darin müssen(!) zunächst mal per se elktrisch neutral, also ungeladen sein.
Erst wenn diese Atomsorten eine Verbindung mit den anderen eingehen, kann es sein, daß Elektronen übertragen werden.
Atome, die Elektronen abgeben, sind danach positiv geladen. Atome, die Elektronen aufnehmen, sind danach negativ geladen.
In den Hauptgruppen I bis VIII (aufpassen, das ist etwas anders gezeichnet als in deinem PSE) ist die Gruppennummer immer gleich der Anzahl an Außenelektronen.
Für I bis III ist es leichter, ein bis drei Elektronen abzugeben. Alle Atomsorten hier werden also positiv werden (=Kationen)
Für VI bis VIII ist es leichter, ein bis drei Elektronen aufzunehmen. Alle Atomsorten hier werden also negative werden (=Anionen)
Die Antriebskraft dahinter ist die Oktettregel (kannst du ja mal googeln)
m.f.G.
anwesende