Welche Valenzsteichformel ist die Richtige?
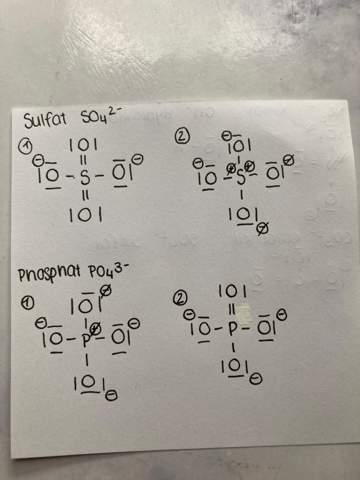
Hallo ich schreibe morgen einen Test im Fach Chemie. Unter anderem geht es dabei auch um das Aufstellen von Valenzstrichformeln von Molekülionen, bei Sulfat und Phosphat habe ich dabei jedoch Probleme. Falls sich hier jemand mit diesem Thema auskennt und auch eine verständlich Begründung liefern kann, würde ich das wirklich sehr wertschätzen und es wäre sehr wichtig und hilfreich für mich!
1 Antwort

Moin,
tja, das ist tatsächlich nicht ganz einfach, weil beide von dir eingestellten Formeln hier und da herumspuken.
Ich halte jeweils die Darstellung mit den Einfachbindungen für korrekt, weil es den Atomen relativ „wurscht” ist, ob sie eine Formalladung haben, so lange sie auf eine gefüllte Außenschale kommen. Und das kommt hier auf jeden Fall hin (Oktettregel ist überall erfüllt).
Bei den Darstellungen mit den Doppelbindungen wurde früher immer angeführt, dass bei größeren Atomen (ab Periode 3) auch die d-Orbitale für Bindungen genutzt werden können. Aber das halte ich (nach wie vor) für eine Verlegenheitsausrede, weil die Energiezustände dieser Orbitale doch einen noch ziemlichen Unterschied zu den p-Orbitalen haben (zumindest bei Phosphor oder Schwefel, um die es hier ja geht).
Es bleibt ungeklärt, wieso diese Atome auf einmal zehn oder sogar zwölf Valenzelektronen haben können. Dagegen spricht aber, dass die Bindungen zum Beispiel im Sulfat-Anion nicht nur alle gleich lang und gleichwertig sind, sondern auch, dass es eine tetraedrische Geometrie hat. All das spricht gegen die klassische Variante der Darstellung mit den Doppelbindungen und für die mit den vier Einfachbindungen und den Formalladungen.
LG von der Waterkant
