Oxidationszahlen in Adrenalin?
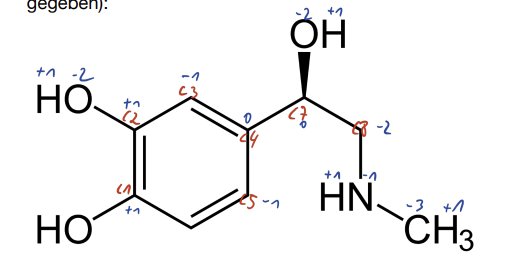
Warum nimmt Stickstoff (N) kein Elektron von C auf, bzw. warum hat unten rechts das Kohlenstoff-Atom (C) die OX-Zahl -3 und nicht -2, da das N-Atom ja eine höhere Elektronegativität besitzt? Gleiches gilt für C8, hier müsste es -1 eig. sein.
Ansatz: N ist ja in der 5. Hauptgruppe, braucht also nur 3 Elektronen, um die Oktettregel zu erfüllen. Es teilt sich mit beiden C's ein Elektronenpaar, bekommt von diesen also zwei und von H nimmt es das Elektron zu sich, da eben nur eins da ist und N viel höhere EN besitzt. Problem in der Theorie: Wir haben mit der freien Doppelbindung nur 5 Elektronen zusammenbekommen, anstatt 8. Ich bin gerade etwas verwirrt und würde mich sehr um eine Klarstellung freuen :D
Dieser Ansatz kann allerdings keinen Sinn ergeben, da O dann das Elektronenpaar mit C sich teilen müssten.
1 Antwort

Stickstoff hat, wenn es nur mit C- und H-Atomen verbunden ist, die OZ -3. In deiner Zeichnung sins die OZ also schlicht falsch.
Das Methyl-C-Atom ganz rechts hat entsprechend -2 und das C-Atom über dem N-Atom -1.

Ordnung in den Kopf gebracht haha, ich bedanke mich :D