Korrosion und Korrosionsschutz Versuch ?
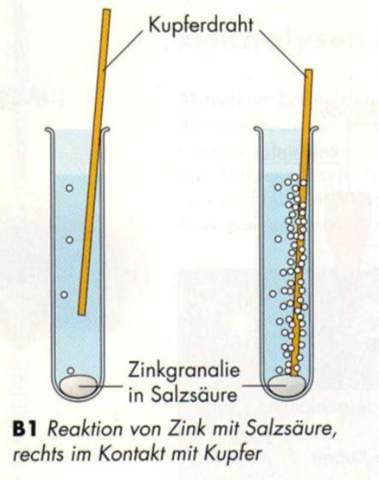
Hallo kann mir jemand den folgenden Versuch (s. Bild) anhand der Korrosion und des Korrosionsschutzes erläutern.
Ich verstehe es einfach nicht.
2 Antworten

Das ist ein Beispiel von der Kontaktkorrosion (2. Bild).
Zn kontaktiert mit Kupfer. Zn hat weniger Potential als Kupfer. Zn ist eine Anode, Kupfer ist eine Kathode. Man ensteht ein galvanisches Element. Die Elektronen gehen von Anode nach Kathode. Und dort (auf dem Kupfer) nehmen H+-Ionen diese Elektronen ab.
(A) Zn/Zn2+//(Cu) 2H+/H2 (K)
Die Enstehung des Wasserstoffs geht stärker als im ersten Fall. Auf dem 1. Bild geht eine Reaktion:
Zn +2H+ => Zn2+ + H2

Naja du hast doch wohl schon wa von der Spannungsreihe gehört?

Gut und jetzt überleg dir mal welches Metall eher von der HCl gelöst wird und Ionen bildet...


Genau weil es unedler ist. Das bedeutet also das sich das Zink aufopfert und das Kupfer somit vor der Korrosion schützt. Vielleicht kennst du den Begriff "Opferanode"

Ja hab ich