Wasserstoffbrücken bei Fluormethan?
Hallo, ich wollte fragen, wieso zwischen benachbarten Molekülen von CH3F keine Wasserstoffbrücken entstehen? Theoretisch könnten sich doch zwischen den H-Atomen und den freien Elektronenpaaren der F-Atomen benachbarter Moleküle Wasserstoffbrücken bilden?
Freundliche Grüsse
2 Antworten

Nein. Wasserstoffbrückenbindungen erfordern ein stark polar gebundenes H-Atom. Das gibt es nur als O-H, N-H oder F-H. Der Wasserstoff ist aber an C gebunden, wobei die Bindung wegen dem F nur schwach polar ist.

Es heißt Wasserstoff-Brückenbindung. Der Wasserstoff ist die Brücke. Zudem habe ich geschrieben: ...ein stark polar gebundenes H-Atom.
Es sind nicht die O-Atome im Wasser, die die Brückenbindung bewirken!
Nur das H wird von wechselnden O-Atomen gebunden (siehe Bild). Das O-Atom hat freie Elektronenpaare, an die sich das H binden kann, wobei die alte Bindung beim alten O als freies Elektronenpaar zurück bleibt. Das geht oft und schnell hin und her. Das H ist also fast wie der Tennis-Ball zwischen zwei Spielern, die dadurch auch locker "zusammen halten".
Bild im folge-Post...

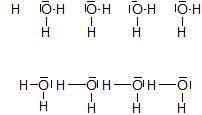
Wasserstoffbrückenbindung "Momentaufnahme".
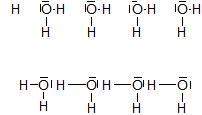
Vielen Dank für Ihre Antwort!
Leider verstehe ich es noch nicht ganz. Was meinen Sie genau mit Wasserstoffbrücken erfordern ein stark polares H-Atom?
Nach meinem Verständnis bilden Wassermoleküle ja Wasserstoffbrücken von den O-Atomen eines Moleküls zu den H-Atomen eines benachbarten Moleküls. Wieso könnten bei CH3F Molekülen, die F-Atome eines Moleküls nicht Wasserstoffbrücken zu H-Atomen eines anderen benachbarten Moleküls bilden? Ich meine Flour hat ja eine grössere Elektronegativität als Sauerstoff.
Muss man um herauszufinden, ob Wasserstoffbrücken gebildet werden die Elektronegativität eines Moleküles gesamthaft anschauen?
Freundliche Grüsse