Wasser im Vergleich zu anderen Nichtmetalloxiden?
Wir behandeln in Chemie gerade das Thema Wasser. Dazu haben wir Aufgaben bekommen. Kann mir vllt. jemand helfen? Wir sollen Wasser in 7 Eigenschaften mit anderen Nichtmetalloxiden (möglichst allgemein) vergleichen und ein Resumee schreiben. Wüsste da jemand etwas? (6, Warum ist Wasser ein besonderes Oxid(im Bild))

5 Antworten

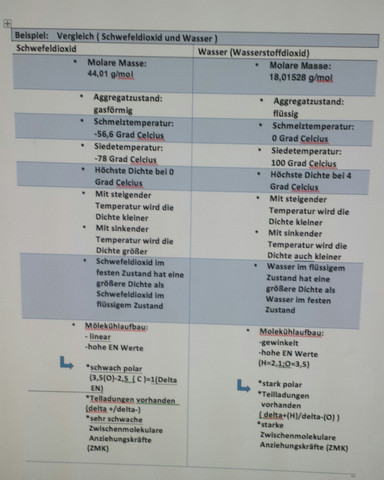
Wir mussten mal als HA in Chemie tabellarisch auch Wasser mit anderen Nichtmetalloxiden vergleichen(Siehe unten Bilder).
Du sagtest ja auch ,dass du ein Resümee schreiben musst :
Wasser weicht sehr von charakteristischen Eigenschaften von Nichtmetalloxiden. Z.B. hat sie eine hohe Siede-und Schmelztemperatur, hat die höchste Dichte bei 4 Grad Celsius, festes Wasser (Eis) hat eine geringere Dichte als flüssiges Wasser, etc..
Diese besonderen Eigenschaften sind mit dem Aufbau der Moleküle zu erklären.Denn die Wassermoleküle sind gewinkelt aufgebaut, sind eine polare Bindung, sind einen Dipol (haben ein plus und Minuspol).
Durch ihre Polarität sind starke Anziehungskräfte zwischen den Wassermolekülen vorhanden. Diese Anziehungskräfte nennt man Wasserbrückenbindungen. Dies erklärt auch die hohe Siede-und Schmelztemperatur.
Hoffe ich konnte dir weiterhelfen;D


ich hab mal eine frage bei dem ersten bikd steht ja das wasser im flüssigen zustand eine größere dichte als im festen zustand hat aber müsste die dichte nicht im flüssigen wie im festen zustand ähnlich ider sogar fast gleich denn sie wird ja bei hoher und niedriger temperatur kleiner oder liege ich gerade komplett falsch

Ich erkläre erstmal meine aussage, dass Wasser im flüssigen Zustand eine größere Dichte hat als beim festen Zustand.
Du kennst das Phänomen bestimmt auch von Gewässern im Winter. Die Oberfläche bei Gewässern friert bei 0 Grad Celsius zu. Und dieses Eis (Wasser im festen Zustand) sinkt ja nicht zu Boden, sondern bleibt oben an der Oberfläche und darunter ist flüssiges Wasser. Eigentlich ist es ja so, dass ein Feststoff in einer Flüssigkeit zu Boden sinkt, weil sie eine größere Dichte als die Flüssigkeit hat. Denn die Teilchen in einem Feststoff sind ja fest aneinander geordnet, bewegen sich kaum, und wegen dieser Anordnung ist auch fast keine Lücke zwischen den Teilchen. Also, wenn dass Volumen klein ist, heißt es, dass die Dichte sehr groß ist.
Aber bei Wasser ist es anders. Im flüssigem Zustand bewegen sich die Teilchen, aber sie sind nahbeieinander und haben Kontakt zueinander. Im festen Zustand nehmen die Teilchen(Moleküle) aber eine bestimmte Struktur ein. Dies ist eine hexagonale Struktur(Kristall). Bei dieser Struktur schließen sich sechs Wassermoleküle über Wasserstoffbrücken(ZMK) jeweils zu einem Ring zusammen. Durch dieser Ring-Struktur entstehen sehr große Lücken zwischen den Wassermolekülen. Wenn sehr große Lücken zufinden sind heißt es, dass sie ein großes Volumen hat und eine geringe Dichte. Somit bliebt das Eis mit der geringen Dichte bei Gewässern an der Oberfläche und das flüssige Wasser mit der größeren Dichte ist darunter.
Die Aussage von dir, dass die Dichte mit wachsender und sinkender Temperatur kleiner wird stimmt. Die Aussage beschreibt eher eine andere Besonderheit von Wasser und hat weniger damit zu tun, dass Wasser im flüssigen Zustand eine größere Dichte hat als beim festen Zustand.
Hoffe ich konnte deine Frage beantworten;D

Oxide sind alle Verbindungen die O2 enthalten wie CO2, H2O2 usw. Wasser ist aufgrund vieler Eigenschaften Besonders. Es hat eine Dichteanomalie und ist sehr stark durch Wasserstoffbrücken gebunden und hat ein amorphen Charakter. Andere Oxide reagieren oft Sauer, Wasser kann sowohl sauer als auch basisch wirken.

Oxide sind Verbindungen, die O enthalten, je nach Stöchiometrie unterschiedlich viele. z.B.: CO, CO2, SO3, P2O5, N2O, NO, NO2 usw.
Amorpher Charakter ???

Hallo cxlxnxw
einige Sachen sind ja schon genannt worden, daher noch diese:
Wasser ist:
- lebensnotwendig
- ungiftig
- universelles Lösemittel
- (löscht den Durst)
LG

dann geh mal auf wicki und vergleiches in einigen punkten z.B. siedepunkt /schmelzpunkt / leitfähigkeit.....
und dann guck dir mal an, ob es herraussticht. wenn dir das auffällt kannst du dir das mal unter den gesichtspunkt wasserstoffbrückenbindung angucken.

Wasser ist flüssig Dichter als fest so viel weiß ich und es ist lipophob.
Es ist außerdem ein Treibhausgas und kann auf natürliche Weise nur sehr schwer gespalten werden mehr weiß ich aber nicht.


Doch, sogar das wichtigste/wirksamste.
Nur verringert sich die Wirkung meinst schnell wieder, wenn das Wasser sich wieder niederschlägt.
dankeschön du hast mir echt weitergeholfen🙈