Warum sind Abstände der Elektronenbahnen im Bohr´schen Atommodell nach außen hin geringer?
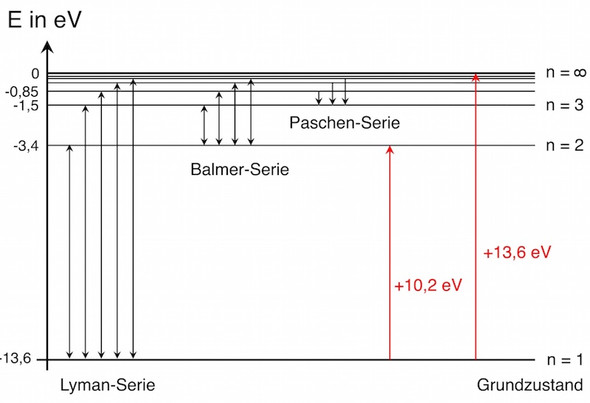
Ich habe ein Bild angefügt welches zu meiner Frage passt. Die Bahnenergien werden mit zunehmenden Abstand zum Atomkern immer größer, aber warum werden die Abstände zueinander immer kleiner?
Wäre toll wenn mir das jemand erklären könnte! Danke :)
4 Antworten

Die Energie, die nötig ist, um ein Elektron komplett vom Atomkern zu trennen, ist endlich, sonst könnte man das Elektron nicht aus dem Einflußbereich des Kerns entfernen.
Unterhalb dieses Niveaus gibt es aber theoretisch unendlich viele Bahnen mit unterschiedlichen Energieniveaus (die irgendwann aber kaum noch experimentell nachweisbar sind), deren Abstände müssen also zwangsläufig geringer werden.

So ist nun einmal die Natur.
Bei höheren Energieniveaus sind die Abstände so klein, dass man kaum mehr von Energiestufen sprechen kann sondern von kontinuierlichen Energien.
Die Werte für die Energien bzw. die Abstände ergeben sich aus der Balmer-Formel bzw. aus den Formeln zur Berechnung der Energien / Energiedifferenzen im Bohrschen Atommodell.
In der Klammer steht (1/m² - 1/n²). Daraus ergeben sich bei zunehmenden Quantenzahlen immer kleiner Abstände zwischen zwei Energiestufen.


weil die energiniveaus wie 1/n² gehen
Weil das Elektron, je weiter es vom Kern entfernt ist, immer "freier" wird. Freie Elektronen haben aber kontinuierliche Energiezustände.