Warum sieht die Lewis Struktur von Thiosulfat so aus?
Hey :)
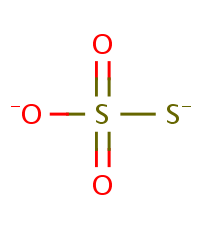
Ich habe die Lewis Struktur von Thiosulfat gezeichnet und meine negativen Ladungen an zwei O-Atomen plaziert. Aber ich finde im Internet nur diese Struktur mit einem Minus an dem Schwefel und eines an dem Sauerstoff. Aber O ist elektronegativer als S. Warum ist das so?
Thx!
2 Antworten

Also bei solchen Sachen sag ich immer gerne:
Ist halt stabiler so. Quantenmechanik sagt das. Ist nicht immer mit einfachen Konzepten zu erklären. Verschiedene Faktoren spielen sich gegeneinander aus.
Hier würde ich aber trotzdem sagen, dass eine Schwefel-Schwefel-Doppelbindung nicht besonders vorteilhaft ist. Elemente der 3. Periode mögen es nicht mehr so sehr aufgrund ihrer diffuseren Orbitale, miteinander Mehrfachbindungen einzugehen. Ich weiß, man könnte hier sich auch eine Struktur mit Formalladungen formulieren, aber ein gewisser Doppelbindungsanteil wäre sicher vorhanden. Dies ist für S=O deutlich besser als für S=S. Das spricht also eindeutig für diese Struktur.
Also einfach so lernen. Gibt viele Sachen in der Stoffchemie, die man einfach so hinnehmen muss und die man sich schwer herleiten kann, weil eben verschiedene Effekte beteiligt sind.
