Rutherford Atommodell Aufgabe?
Hallo zusammen,
ich brauche dringen Hilfe bei meinen Chemie Hausaufgaben. Es würde mich freuen wenn ihr jede frage beantworten könnt. Die Fragen sind unten.
Danke im Voraus
3 Antworten

Moin,
L16 & 17 & 18:
Rutherford (und seine Mitarbeiter) beschossen einen hauchdünne Goldfolie mit alpha-Teilchen. Um die Goldfolie herum verläuft ein Zinksulfid-Leuchtschirm. Das Zinksulfid leuchtet auf, wenn alpha-Teilchen darauf stoßen. Rutherford und seine Mitarbeiter beobachteten nun, dass die alpha-Teilchen zum größten Teil einfach durch die Goldfolie gingen, weil es hinter der Goldfolie direkt auf der Flugbahn der alpha-Teilchen am häufigsten und intensivsten aufleuchtete. Ein paar alpha-Teilchen wurden mehr oder weniger stark abgelenkt und nur etwa jedes 10.000-ste alpha-Teilchen wurde zurück geworfen, „prallte also quasi von der Goldfolie ab”.
Da alpha-Teilchen selbst positiv geladene Teilchen sind, schloss Rutherford aus diesen Beobachtungen folgendes:
1. Atome bestehen aus einem winzigen Kern und einer im Vergleich dazu riesigen Hülle. Der Atomkerndurchmesser ist etwa 10.000-mal kleiner als der Hüllendurchmesser.
2. Die Hülle besteht im Grunde aus Nichts. Der Kern ist dagegen massiv und positiv geladen.
3. In der Hülle befinden sich die negativ geladenen Elektronen.
4. Deshalb konzentriert sich also fast die gesamte Masse sowie die positive Ladung auf den Atomkern. Die Hülle hat so gut wie keine Masse, weil sie einerseits aus Nichts besteht, andererseits die Elektronen auch so gut wie keine Masse haben (im Vergleich mit dem Atomkern).
5. Das Atom erscheint nach außen hin ungeladen, weil sich die negative Ladung der Elektronen in der Hülle und die positive Ladung im Kern gegenseitig in ihrer Wirkung aufheben (kompensieren).
Diese neue Annahme über den Bau der Atome erklärt einerseits, warum die meisten alpha-Teilchen durch die Folie hindurch fliegen, weil sie dann einfach die Hülle aus Nichts durchqueren.
Die abgelenkten alpha-Teilchen fliegen dagegen dicht an den Atomkernen vorbei. Da die alpha-Teilchen selbst positiv geladen sind und die Kerne ebenso, stoßen sich die gleichsinnigen Ladungen voneinander ab, so dass die alpha-Teilchen abgelenkt werden.
Wenn aber ein alpha-Teilchen direkt auf einen winzigen Kern stößt, wird es zurück geworfen, weil der Kern einerseits positiv geladen und andererseits massiv ist.
Da nur circa jedes 10.000-ste alpha-Teilchen zurück geworfen wird, kann man daraus schließen, dass der Kern ungefähr 10.000-mal kleiner als das Atom selbst ist.
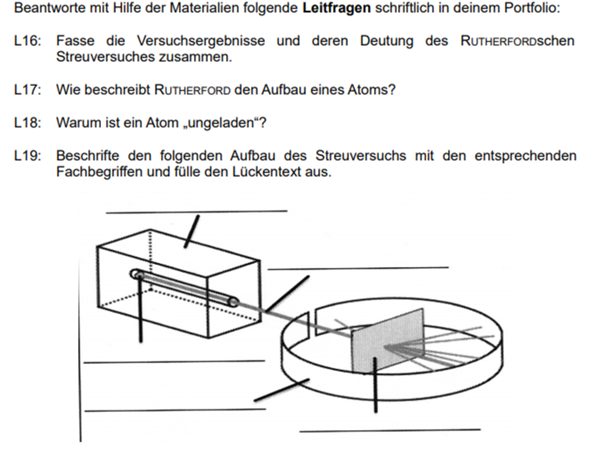
L19 (von oben nach unten):
- Bleiblock
- alpha-Teilchenstrahl
- radioaktives Präparat (alpha-Strahler)
- Zinksulfid-Leuchtschirm
- Goldfolie
Fehlende Wörter im Lückentext:
- Gold
- passieren (durchqueren; durchfliegen)
- abgelenkt
- (Atom-)Kern
- (Atom-)Hülle
- Kerne
- zurück geworfen
LG von der Waterkant

Schon klar. Aber du kannst doch lesen. In L16 solltest du die Ergebnisse des Versuchs zusammenstellen und deuten.
In den Punkten 1., 2. ... bis 5. steckt dann die Vorstellung Rutherfords zum Bau der Atome.
Und der Punkt 5. ist die Antwort auf L18...
Was ist daran so schwer?

Lückentext:
Gold, durchqueren, abgelenkt, Kern, Hülle, Kerne, zurück geworfen
Ich hoffe alles stimmt
LG Hildeberta

Danke sehr Hilfreich. Können Sie mir L16, L17 und L18 auch erklären/beantworten

L16
Bei dem Versuch hat man festgestellt, dass Die meisten Strahlen durch die Folie hindurch gehen, einige abgelenkt werden und ein paar einzelne wieder zurückgeworfen werden.
Dadurch hat man herausgefunden, wie ein Atom aufgebaut ist. Der atomkern muss fast die Gesamte Masse des Atomes ausmachen, ist jedoch im Vergleich zur Hülle sehr klein. Das fand man heraus, da die Strahlen, die auf den Kern treffen abgelenkt werde und das sind sehr wenige. Die leicht abgelenkten sind nahe m Atomkern vorbeigeflogen. Die meisten Strahlen sind jedoch nahezu gerade durch die Folie hindurch gegangen. Somit wurde bewiesen, dass Die Atomhülle fast keine Masse hat, jedoch deutlich größer als der Atomkern ist.


L18
Das Atom ist ungeladen, da es weder positiv noch negativ geladen ist. Das Atom hat genauso viele negativ geladene Elektronen, wie positiv geladene Protonen. Wie viele Neutronen es besitzt ist für die Ladung egal.

Da das Kern durch die Strahlung stabiler wird, wird die ganze atomm... Sike, ich weiß es selber nicht

Danke, mein Problem ist nur zu erkennen, welche Aufgabe, zu welchem Teil gehört.