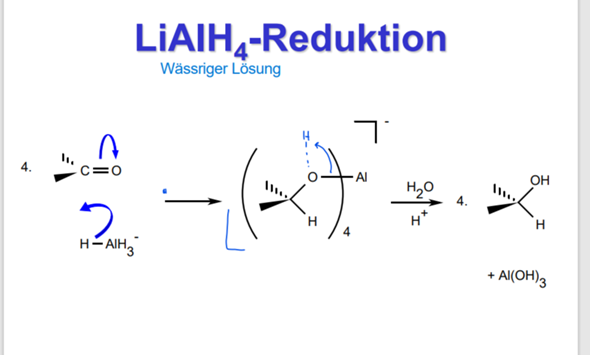
LiAlH4-Reduktion Mechanismus?
Ok, es kommt so, dass sich das Zeug viermal ans Aluminium bindet. Danach wird es abgespalten.
Meine Fragen:
- Das H2O geht in die Reaktion, weil es eine wässrige Lösung ist, oder? Aber woher kommt das H+?
- Warum setzt sich am Ende nicht wie davor 4 mal OH an das Al, sondern nur dreimal?
- Wenn das OH am Al vom H+OH-, also Wasser ist, wohin kommt das Proton des Wassers im letzten Schritt? Okay, ein Proton sorgt dafür, dass das O an der abgespaltenen Gruppe zu OH wird, aber am Reaktionspfeil sind zwei Protonen, eins vom Wasser und das andere H+?
2 Antworten

Hi,
1) aus dem Wasser
2) Die Formel für Aluminiumhydroxid ist nun mal Al(OH)3, weil Aluminium nun mal dreiwertig ist. Du hast gedanklich aber das Li vergessen, denn das wird das von dir übersehene 4te LiOH
3) in einer sauren, wässrigen Lösung sind unendlich viele H+ und H2O vorhanden. Deren Konzentration ist vorher und nachher also praktisch identisch. In so einem Fall schreibt man das nur auf den Reaktionspfeil.
Denke ganz einfach:
LiAlH4 überträgt 4 mal je ein H- an das Carbonylkohlenstoff
H2C=O + (H-) ---> H3C-(O-)
Dieses holt sich ein H+ aus dem Wasser
H3C-(O-) + H2O --> H3C-OH + (OH-)
Wie du schon sagtest, passiert das 4 mal, also entstehen auch 4mal (OH-). Diese reagieren mit AL und Li zu Al(OH)3 und LiOH

LiAlH4 ist LithiumAluminiumHydrid. Der Wasserstoff ist negativ geladen. Bei der Reaktion wird die Ketogruppe zur Alkohol Gruppe reduziert. Und eine Reduktion bedeutet eine Aufnahme von Elektronen. Somit "verliert" der Wasserstoff die Elektronen und wird somit formal zum Proton. Aber ich glaube das die anderen Kollegen, dass besser erklären können.