Antibindendes Molekülorbital?
Ich habe zwei Fragen zu dem Thema.
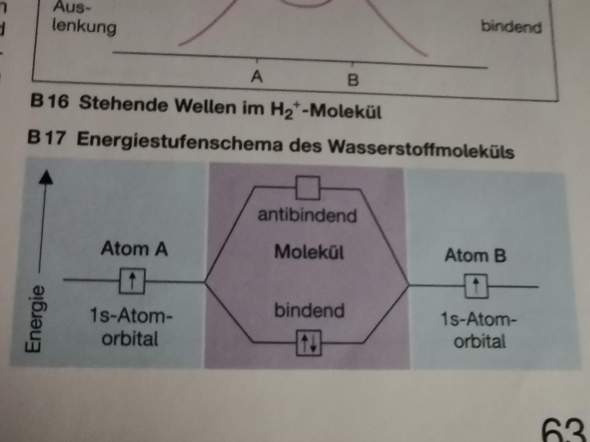
1. Wenn wir zu diesem Wasserstoff Molekül Energie zuführen, wandert ein Elektron in das energetisch höhere Molekülorbital(antibindendes MO). Somit ändert sich die Elektronenwelle des Elektrons und die Wellen heben sich auf und das Molekül spaltet sich in zwei H-Radikale. IST DAS GANZE SO RICHTIG?
2. Die beiden Elektronen im bindenden Zustand befinden sie sich unten im Kasten in einem Molekülorbital oder in zwei Molekülorbitalen also jeweils in einem 1 s Molekülorbital?
1 Antwort

zu 1, richtig
zu 2 - die beiden ELektronen befinden sich in einem Molekülorbital, das die Aufenthaltswarscheinlichkeit der Elektronen zwishcen den beiden Atomkernen festlegt.
Diese Molekülorbitale heißen sigma-Orbitale, sind also keine Atomorbitale, nur aus denen entstanden (sind ja auch energieärmer..)

Eigentlich änderst du den Energieinhalt der beiden Elektronen, indem du das Elektronenpaar auf das nächsthöhere erlaubte Energieniveau hebst.
Dieser Zustand kann erneut durch ein Molekülorbital beschrieben werden, was letztlich eine Lösung der Schrödinger-Gleichung ist und dann natürlich auch einer höheren Energie entspricht.
Kennst du die LCAO und die Psi-Funktion?

Zu eins noch mal. Warum ändert sich die Elektronenwelle des einen Elektrons, wenn dem Molekül Energie zugeführt wird?