Wie funktioniert die Lewis-Formel?
Ich bereite gerade ein Referat für kurz nach den Ferien vor und müsste dafür mal verstehen wie die Lewis Formel funktioniert. Nehmen wir mal ein angegebenes Beispiel: Chlorwasserstoff ist als Summenformel HCl. Als Lewis-Formel ist es H-Cl, wobei um das "Cl" drei Striche drumherum sind. Ich weiß nur, dass es Punkte und Striche gibt, ein Punkt bedeutet 1 und ein Strich 2. Die Frage ist nur: 1 oder 2 was? Ich dachte zuerst es würde sich nach der Hauptgruppennummer richten, dummerweise wären 3 Striche aber 6 und Chlor ist in der 7.Hauptgruppe! Wäre lieb von euch wenn ihr mir helfen könntet :)
3 Antworten
Hi,
diese "1 oder 2" sind die Elektronen :)
_______________________________________________________________
Ein Element hat eine entsprechende Anzahl von Elektronen auf der äußersten Schale - darüber gibt die Hauptgruppe Auskunft. Bleiben wir bei deinem Beispiel.
H steht in der ersten Hauptgruppe, hat also ein Elektron in der äußersten Schale. Cl steht in der siebten Hauptgruppe, hat also sieben Elektronen auf der Außenschale.
Nun reagieren die beiden. Passieren tut Folgendes:
a) Chlor nimmt ein Elektron auf:
Cl2 + 2e(-) -> 2 Cl(-)
b) Wasserstoff gibt Elektronen ab:
H2 -> 2 H(+) + 2 e(-)
DIe Gesamtgleichung ist:
H2 + Cl2 -> 2 HCl
Die Elemente haben das Bestreben nach einer vollen Außenschale, weshalb sie in den meisten Fällen Elektronen aufnehmen oder abgeben.
Soviel zum Hintergrund. Was heißt das jetzt für die Lewis-Formel?
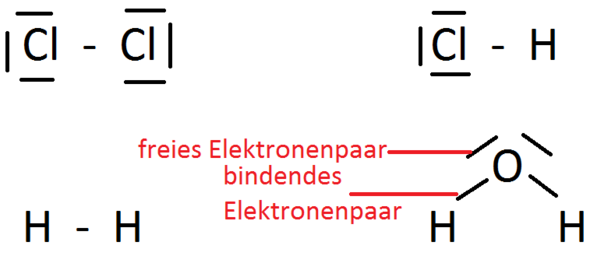
Ganz einfach: Wir haben ein bindendes Elektronenpaar. Und genau DAS ist der Strich zwischen Wasserstoff und Chlor. Im Anhang mal die Lewis-Formeln für Chlor und Wasserstoff und für Chlorwasserstoff.
Nun Hat das Chlor ja noch sechs Elektronen, also drei freie Elektronenpaare. Das sind diese Striche um das Chlor.
Soweit klar? Okay, dann weiter zu einer allgemeineren Erkläreung dazu.
_______________________________________________________________
Die Lewis-Formel
Die Lewis-Formel ist eine Schreibweise der Verbindung, die dir die Struktur einer Verbindung verdeutlicht. Allerdings gibt die keine Auskunft darüber, wie das Molekül räumlich gebaut ist. Durch die Elektronenpaarabstoßung erhalten Moleküle ihre "Form" die beiden H's stoßen sich ab, ebenso die freien Elektronenpaare. Bei CO2 liegt die größtmögliche Abstoßung bereits vor, deshalb ist es linear.
Vorgehen beim Zeichnen einer Lewis-Formel
Ich werde dir das Vorgehen hier nochmal am Beispiel Wasser verdeutlichen.
=> Zuerst schaust du, in welcher Hauptgruppe das Element steht. Die Hauptgruppe gibt Auskunft darüber, wie viele Elektronen sich auf der äußersten Schale des Elements befinden. Schaust du in das Periodensystem, so wirst du feststellen, dass Wasserstoff (H) in der ersten und Sauerstoff (O) in der sechsten Hauptgruppe steht.
=> Davon ausgehend kannst du die Struktur der einzelnen Elemente zeichnen. Im Anhang siehst du die Struktur von Wasserstoff und Sauerstoff. Bei Sauerstoff wird dir Auffallen, dass dort zwei Striche und zwei Punkte sind. Ein Punkt steht für ein einzelnes Elektron, ein Strich für ein Elektronenpaar.
=> Du fragst dich jetzt sicher, warum ich da nicht drei Striche bei Sauerstoff gemalt hab? Das ist ganz einfach: Bei der Lewis-Formel wird das möglichst symmetrisch gezeichnet.
=> Dies zeigt auch immer an, wie oft ein Element binden kann: Die Anzahl von Punkten zeigt, wie oft ein Element binden kann. Es kann höchstens vier mal binden. Sauerstoff kann zwei mal binden, Wasserstoff jeweils einmal (eigentlich ist es H2 da Wasserstoff ein BrINClHOF-Tier ist).
=> Wenn eine Verbindung entsteht, ist immer die Oktettregel erfüllt: Jedes Element hat acht Elektronen auf seiner äußersten Schale. Bei Wasserstoff reichen zwei Elektronen, damit die Oktettregel erfüllt ist, da es in der ersten Periode nur zwei Hauptgruppen gibt.
Elektronenpaare
=> Die Lewis-Formel von Wasser siehst du auch im Anhang. Dort sind auch die Begriffe freies und bindendes Elektronenpaar aufgeführt. Ein freies Elektronenpaar ist ein Elektronenpaar, das nicht verbunden ist. Ein bindendes Elektronenpaar ist ein Elektronenpaar, welches zwei Elemente miteinander verbindet.
=> In diesem Zusammenhang tauschen dann auch die Begriffe Einfachbindung, Doppelbindung und Dreifachbindung auf.
=> Bei einer Einfachbindung ist nur ein bindendes Elektronenpaar zwischen zwei Elementen. Dies ist bei H2 der Fall.Bei einer Doppelbindung sind zwei bindende Elektronenpaare zwischen zwei Elementen. Dies ist bei O2 der Fall.
=> Bei einer Dreifachbindung sind drei bindende Elektronenpaare zwischen zwei Elementen - bei N2 ist dies der Fall.
Dipole
=> Bei Wasser würde O ein δ- und die beiden H's ein δ+ bekommen. Bei den δ's spricht man von Partialladungen.
=> Das δ- kriegt immer das Element, welches die höhere Anzahl an Protonen hat, da es die Elektronen aufgrund der Anziehungskräfte näher zu sich "ran zieht". Die eine Seite ist somit etwas positiver, die andere Seite etwas negativer geladen.
=> Wasser ist ja ein gewinkeltes Molekül. Wäre es linear, so wie z.B. CO2, und wäre es so gebaut, dass sich die Partialladungen aufheben, wäre es kein Dipol. Da man durch das Wassermolekül aber eine Achse legen kann, ist es ein solches.
Elektronegativitäten
=> Jedem Element kann man eine bestimmte Elektronegativität zuweisen. Der Physikchemiker (oder wie das heißt) Pauling hat eine solche Tabelle erstellt, wobei er Fluor mit einer 4,0 versehen hat - dieses Element hat nämlich nur zwei Außenschalen und dafür verhältnismäßig viele Protonen, also zieht es auch entsprechend stark.
=> Mit den Elektronegativitäten lässt sich ebenfalls feststellen, ob ein Dipol vorliegt. Das elektronegativere Element kriegt das δ-, das positivere (mit der kleineren Elektronegativität) das δ+.
=> Man kann nun auch ΔEN, die Elektronegativitätsdifferenz, bestimmen. Ist diese kleiner als 1,7 , so liegt eine polare Bindung vor.Ist diese allerdings größer als 1,7 , so liegt eine Ionenbindung - meist ein Salz vor. HF aber hat eine größere ΔEN als 1,7 und ist kein Salz. Ausnahmen bestätigen die Regel ;-)
Da wären wir auch schon bei den Van-der-Waals-Kräften und der Wasserstoffbrückenbindung. Allerdings wäre das hier zu viel. Außer natürlich du willst es erklärt haben. Die Lewis-Formeln, die damit zusammenhängenden Dipole, Wasserstoffbrückenbindungen, Elektronegativitäten etc. umfassen ein weites Spektrum.
_______________________________________________________________
Ich werde es erstmal dabei belassen. Bitte entschuldige meinen langen Text - wenn ich erkläre, dann schon ausführlich.
Ich hoffe, dass ich dir mit meiner Antwort wenigstens ein wenig helfen konnte. Bei Fragen melde dich, Chemie ist mein Leistungskurs und mein bestes Fach :)
LG
ein Punkt bedeutet 1 freies Valenzelektron und ein Strich 2.
ist der Strich zwischen zwei Elementen zeigt er die Bindung mit 2 Elektronen an.
Aber das erklärt zur Abwechslung auch Wikipedia mal relativ einfach :D
https://de.wikipedia.org/wiki/Elektronenformel
lg
Außenelektronen
also H hat eins (ein Punkt) und Cl 7 (3 Striche+ein Punkt) und die beiden Punkte werden verbunden, sodass ein Strich entsteht
Also heißt das dass H ja einen Punkt hat wegen der 1. Hauptgruppe und Cl 3 Striche und einen Punkt wegen der 7.Hauptgruppe aber der eine Punkt von H verbindet sich mit dem einzelnen Punkt von Cl sodass daraus ein Strich wird der zwischen H und Cl steht?
Wenn ja dann hab ichs verstanden :)
http://www.eqiooki.de/chemistry/design/to_hydrogen_chloride.png