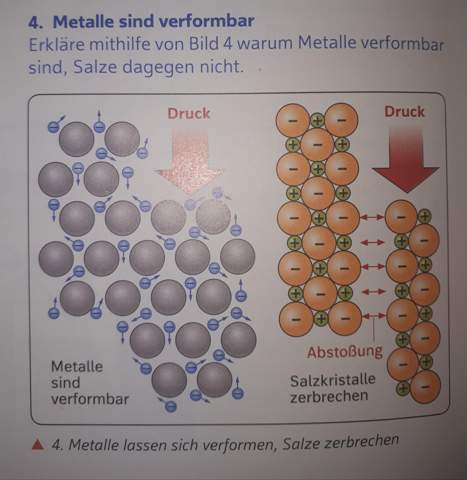
Warum sind Metalle verformbar aber Salze nicht?
1 Antwort

Salze sind über eine Ionenbindung verbunden:
Ein Element neigt dazu, dem anderen ein Elektron zu nehmen und negativiert sich dadurch (Elektronegativität), das andere positiviert sich. Wir erhalten ein Kation (+) und ein Anion (-). Wie du sicher weißt, ziehen sich diese Ladungen an und gleichnamige stoßen sich ab. Es bildet sich ein sogenanntes Ionengitter in dem alles geordnet ist. (Also +/-/+/-/+/ usw....)
Bei einer Metallbindung ist das anders
Metalle sind zunächst viel größer als die anderen Elemente und dadurch auch instabiler. Die Elektronen sind freibeweglich und mischen sich unter die anderen Atomrümpfe (Atomkerne) der Metalle. Das bezeichnet man als Elektronengas.
Wenn man sich jetzt feste Rümpfe (Atomkern) und dann dazwischen freie Elektronen (also eine Art Wolke) vorstellt könnte man gut nachvollziehen, dass Metalle biegsamer sind als Ionenverbindungen.
Konnte ich dir helfen? Wenn du noch Fragen hast, lass es mich wissen


Sonst schau dir mal ein Video von Mai an. (Dr. Mai Thi Nguyen-Kim) Ihr Kanal heißt Mailab und sie hat auch noch einen Lernkanal der heißt musstewissenchemie.
Sehr empfehlenswert

Ich hab die Frage nicht gestellt ;) Mai ist für mich keine Unbekannte ;)
Schöne Antwort :)