Chemie: Lewisformeln hilfe C6h6 / SF6?
Hallo Warum sind bei C6H6 die Elektrone von Kohlenstoff miteinander verbunden aber bei SF6 nicht
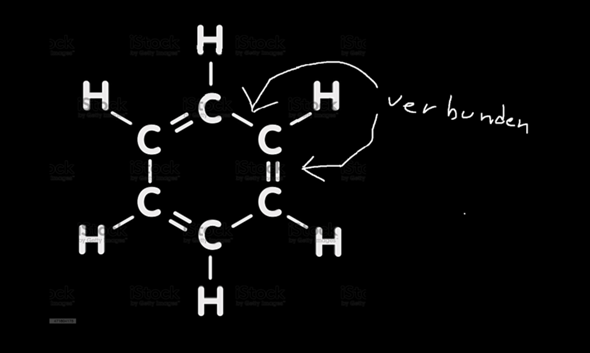
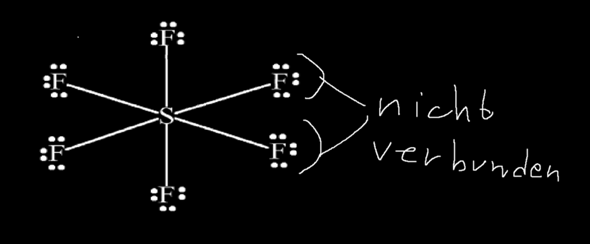
Könnte man zwischen den Flour atomen nicht auch einfach die Elektronen miteinander verbinden?
mfg.
2 Antworten

Von gutefrage auf Grund seines Wissens auf einem Fachgebiet ausgezeichneter Nutzer
Chemie
Benzol ist ein konjugiertes pi-Elektronensystem, daher kann man technisch nicht von Doppel- und Einfachbindungen reden. Eigentlich sind alle Bindungen 3/2 Bindungen, das ist aber schwierig zu zeichnen.
Schwefelhexafluorid bildet kein Pi-Elektronensystem aus, sondern nur 6 Sigma-Bindungen zwischen Schwefel und Fluor.

Von gutefrage auf Grund seines Wissens auf einem Fachgebiet ausgezeichneter Nutzer
Chemie, Elektronen
Weil ein „Querverbindung“ der F-Atome im SF₆ mit der Oktettregel unverträglich wäre (und auch noch ein paar andere Probleme aufwürfe).
Woher ich das weiß:Studium / Ausbildung – Chemiestudium mit Diss über Quantenchemie und Thermodynamik