Ich hab keine Ahnung von Biochemie, oder Biologie, oder Ernährung, daher .... meh, aber dennoch:
Ascorbinsäure ist eine schwache Säure (selbst der pks_1 liegt bei über 4 und der pks_2 ist gleich bei fast 12, also irrelevant), sie liegt im Magensaft also in protonierter Form, nicht als Ascorbatanion vor, diese Zwischenstufe ist hier wichtig, denn um die (Di)Keto-En(di)ol-Tautomerie zu realisieren, muss ein Proton übertragen werden, man spricht auch von Protonentransfertautomerie, was durch den niedrigen pH der Magensäure inhibiert wird.
Ich denke daher, dass die hohe Bioverfügbarkeit von Eisen durch Ascorbinsäure nicht auf die Acidität der Ascorbinsäure zurück zu führen ist und vielmehr auf ihrer Eigenschaft als guter Komplexhemmer, bzw. mäßig schlechter Komplexbildner, beruht. Wie hier zu sehen ist, grabbelt das je freie Elektronenpaar der relevanten Hydroxygruppen sich an das Eisen, hier wahrscheinlich Fe^2+.:
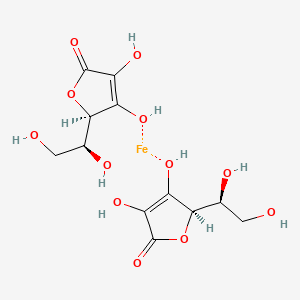
Das Eisen ist in dieser Form quasi versteckt und kann nicht von stärkeren Komplexbildnern, die häufig in Nahrung enthalten sind, man spricht dabei gelegentlich auch von Anti-Nährstoffen, wie Phytinsäure, komplexiert werden, was zur unverwerteten Ausscheidung des Eisens führen würde.
Der Ascorbinsäurekomplex kann hingegen ziemlich leicht durch spätere Oxidation der Ascorbinsäure innerhalb des Verdauungsprozesses zerstört werden, so dass das Eisen verfügbar wird.
Ich denke auch deshalb, dass das hier der Fall ist, da in Eisen-Vit.C-Tabletten auch häufig Äpfelsäure enthalten ist, was für mich ein Hinweis dafür ist, dass die Oxidation der Ascorbinsäure durch Unterbindung der Tautomerie verhindert werden soll.











