Wieso sind trigonale Moleküle achiral?
Ich habe ein Molekül vor mir das wie folgt aussieht (Brenztraubensäure): Das C-Atom hat 3 verschiedene Substituenten: einmal eine Doppelbindung zum O, eine Binudng zu COOH und eine zu einem CH3.
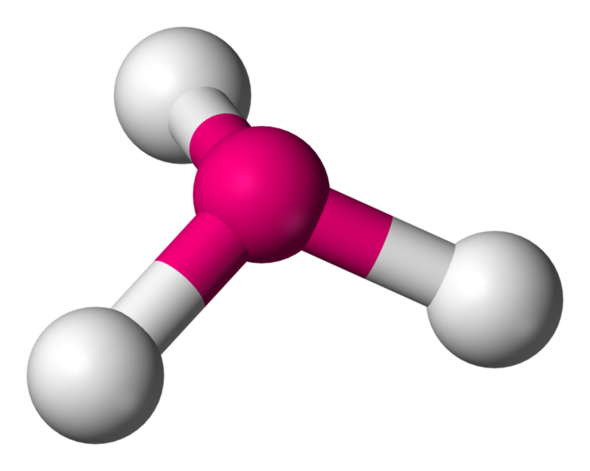
Nun heisst es hier, dass dieses Molekül achiral ist. Das Molekül ist ja trigonal. Sieht also aus wie eine Pyramide. Ich habe mir das ganze mal gebastelt und sehe nicht ein, wie das Spiegelbild mit dem Molekül zur Deckung gebracht werden kann.... Ich habe es in alle Richtungen gedreht., aber es kommt nie die gleiche Pyramide raus... Kann mir da jemand helfen? Ich habe auch kein Video dazu gefunden und kann es mir einfach nicht vorstellen....
Wenn ich die Formel wie folgt aufschreiben möchte: CH3 -- C -- CO2H kommt es dann drauf an ob ich das O oben hin oder unten hin schreibe?
Danke für eure Hilfe!
2 Antworten

- Das zentrale C-Atom ist sp2-hybridisiert und daher planar und achiral.
- Das Molekül hat NICHT die von dir angenommene pyramidale Anordnung.
- Du hast aber recht, WÄRE es pyramidal, dann wäre es auch chiral.

Kohlenstoffatome mit drei Bindungen sind eigentlich immer sp2-hybridisiert und trigonal-planar. Deine Nachfrage ist daher sehr theoretisch. Ich kann mir spontan kein Molekül vorstellen, bei dem das der Fall wäre.
Was ist denn eine "freie Doppelbindung"? Meinst du ein freies Elektronenpaar? Dann wäre das Molekül negativ geladen und das freie Elektronenpaar würde den vierten Platz der formal tetragonalen Pyramide einnehmen. Die Inversionsbarriere zwischen beiden möglichen Enantiomeren ist aber so gering, dass das Molekül wie ein Regenschirm beständig umschlägt. Wikipedia: "Carbanion".
Es gibt Atome, die neben drei Bindungen auch ein freies Elektronenpaar haben und dabei neutral sind. Schlag mal in Wikipedia "Trögersche Base" nach, mit Stickstoffatomen mit drei Bindungen und einem freien Elektronenpaar als quasi vierter Substituent; die spezielle Konstitution verhindert hier das Invertieren der beiden Enantiomere. Auch "Dimethylsulfoxid" ist tetragonal-pyramidal mit einer Doppelbindung in eine Richtung und einem freien Elektronenpaar in eine weitere.

Verschiebt sich bei einer Doppelbindung das ganze nicht auf einen Ebene?

hmm... das C-Atom ist ja sp2-hybridisiert... heisst das dann, dass es planar ist?
... Stimmt, das könnte noch sein.... liegen also alle auf einer Ebene... dann würde es Sinn machen :) Danke dir vielmals!

hmmm wie ist es dann bei C-Atomen, die drei Substituenten haben aber nicht sp2-hybridisiert sind, also keine Doppelbindung haben? Die sind ja dann trigonal pyramidal und nicht trigonal planar, oder?

C ist vierbindig. Ein C-Atom mit drei Substituenten und ohne Doppelbindung existiert aus energetischen Gründen nicht. Aber Du kannst ja mal darüber nachdenken, warum ein tertiäres Amin mit drei unterschiedlichen Substituenten nicht chiral ist: NR'R''R'''
;)
Danke!!
Also wenn das C-Atom drei Substituenten hätte plus eine freie Doppelbindung, dann wäre es chiral, ja?