warum lässt der pH-Wert keine ausreichende Aussage über die säurestärke zu?
Aufgabe: 1-3

Text:



Das ist noch zu aufgabe 2:(hilfe)
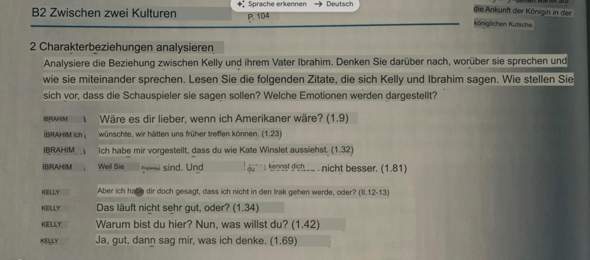
Zu Aufgabe 3 noch:
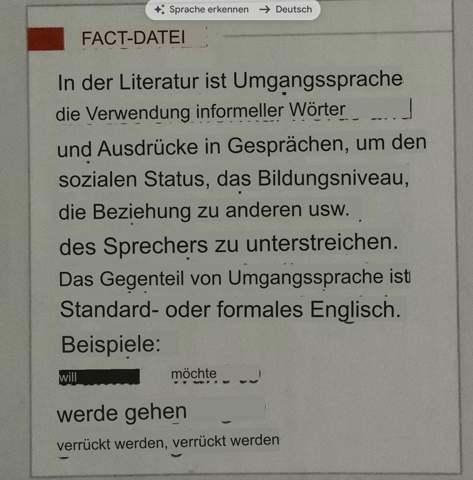
2 Antworten

Weil die Konzentration auch eine Rolle spielt, und gegebenenfalls die Anzahl der übertragenen Protonen.
Salzsäure ist eine stärkere Säure als Zitronensäure. Aber die pH-Werte beziehen sich ja nicht auf die reine Substanz, sondern auf Lösungen unterschiedlicher Konzentration. Für Salzsäure läßt sich der pH-Wert einer 1, 0.1, 0.01, 0.001, … mol/l Lösung einfach als 0, 1, 2, 3, 4, 5, … ausrechnen. Bei der Zitronensäure ist es komplizierter, aber die entsprechenden Zahlen sind 1.55, 2.06, 2.60, 3.22, 3.98, 4.77, …
Du siehst also nicht nur, daß eine 1 mol/l Zitronensäure saurer ist (=einen niedrigeren pH hat) als eine 0.01 mol/l HCl, sondern sogar, daß eine Zitronensäurelösung unterhalb von 10⁻⁴ mol/l saurer ist als eine HCl derselben Konzentration.

Der pH-Wert ist ein Maß der Protonen-Konzentration in einer Lösung. Mehr nicht.
Die Säurestärke hingegen zeigt, in welchem Maße eine Verbindung mit Wasser unter Protolyse reagiert, d.h. Protonen an Wasser abgibt.
Diese beiden Größen sind nicht direkt miteinander verknüpft. Eine hoch konzentrierte Lösung einer schwachen Säure kann denselben pH-Wert haben wie eine gering konzentrierte Lösung einer starken Säure.