Dipol-Molekül von Schwefeldioxid
Ich versteh so eine Teil einer Aufgabe nicht...ich geb jetzt einfach die ganze Aufgabe ein und sag euch dann, was daran ich nicht kapiere:
a) Stelle die LEWIS-Formel von Schwefeldioxid auf. b) Überprüfe die Gültigkeit der Oktettregel. c) Begründe mit dem Elektronenpaarabstoßungs-Modell die gewinkelte Struktur des Moleküls. d) Liegt ein Dipol-Molekül vor? Kennzeichne Ladunsgverschiebungen. e) Schwefeldioxid löst sich sehr gut in Wasser. Dieser Prozess ist ein wichtiger Schritt bei der Entstehung von saurem Regen. Begründe die gute Löslichkeit
Also, ich hätte gerne Antworten für d) und e). Kann mir da irgendwer weiter helfen? Danke schonmal im vorraus!
3 Antworten

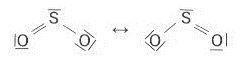
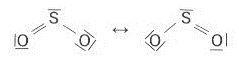
Zu d) Die mesomeren Grenzformeln (siehe Anlage) zeigen eine mögliche Ladungsverschiebung. Diese Grenzformeln stellen aber keine wirklich existierenden Teilchen dar, sondern sind nur „Schreibhilfen“, um den wirklichen nicht mit einer einzigen LEWIS-Formel beschreibbaren Zustand zu beschreiben. Da die Ladungsschwerpunkte bei dem gewinkelten Molekül nicht zusammenfallen, liegt ein Dipolmolekül vor. Das zeigt sich dann auch in der Wasserlöslichkeit.
Zu e) V(Wasser) = 1 L löst bei Zimmertemperatur V(Schwefel(IV)-oxid) = 40 L. Dabei kommt es sofort zur Reaktion
H₂O + SO₂ --> H₃O⁺ + HSO₃⁻ (Es entsteht also keine schweflige Säure)
Zwischen Molekülen mit einem permanenten Dipol wie dem Wasser- und dem Schwefel(IV)-oxidmolekül kommt es aufgrund der unterschiedlichen Ladungsverteilung zu einer Wechselwirkung.

Zu d) http://de.wikipedia.org/wiki/Schwefeldioxid und damit ergibt sich auch die Antwort für e)

Die Anlage bei meiner Antwort wird offenbar nicht korrekt angezeigt. Ich hoffe aber, dass es jetzt klappt.

Das dauert manchmal, bis die richtig angezeigt werden. Hast Du die Seite unter Cache-Umgehung neu geladen?